
Présentation du produit
| Syringaldéhyde Informations de base |
| Présentation Sources naturelles Extraction et isolements Activité biologique et applications Références |
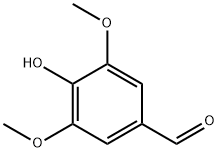
| Nom du produit : | Syringaldéhyde |
| Synonymes : | seringuealdéhyde;Syringylaldéhyde;3,5-Diméthoxy-4-hydroxybenzaldéhyde~4-Hydroxy-3,5-diméthoxybenzaldéhyde;Syringaldéhyde (4-Hydroxy 3,{{ 8}}diméthoxybenzaldéhyde);SYRINGALDEHYDE 99 %;Syringealdéhyde98 %;Syringaldéhyde, 98+ %;Syringealdéhyde 98 % |
| CAS : | 134-96-3 |
| MF : | C9H10O4 |
| MO : | 182.17 |
| EINECS : | 205-167-5 |
| Catégories de produits: | Aldéhydes aromatiques et dérivés (substitués); Bloc de construction; Aldéhydes; Blocs de construction; C9; Composés carbonylés; Synthèse chimique; Blocs de construction organiques; bc0001 |
| Fichier Mol : | 134-96-3.mol |
 |
|
| Propriétés chimiques du Syringaldéhyde |
| Point de fusion | 110-113 degré (lit.) |
| Point d'ébullition | 192-193 degré 14 mm Hg(lit.) |
| densité | 1.013 |
| indice de réfraction | 1,4500 (estimation) |
| FEMA | 4049|4-HYDROXY-3,5,-DIMETHOXY BENZALDEHYDE |
| Fp | 192-193 degrés/14 mm |
| température de stockage. | Conserver dans un endroit sombre, scellé au sec, température ambiante |
| solubilité | Chloroforme, méthanol (légèrement) |
| formulaire | Poudre cristalline |
| pka | 7,80±0,23 (prédit) |
| couleur | Jaune-vert clair à brun |
| Odeur | à 100,00 %. doux plastique boisé tonka sucré |
| Type d'odeur | vert |
| Solubilité dans l'eau | très peu soluble |
| Sensible | Sensible à l'air |
| Merck | 14,9015 |
| Numéro JECFA | 1878 |
| BRN | 784514 |
| La stabilité: | Hygroscopique |
| LogP | 1.30 |
| Référence de la base de données CAS | 134-96-3(Référence de la base de données CAS) |
| Référence de chimie NIST | Benzaldéhyde, 4-hydroxy-3,5-diméthoxy-(134-96-3) |
| Système d'enregistrement des substances de l'EPA | Syringaldéhyde (134-96-3) |
| Information de sécurité |
| Codes de danger | Xn,Xi |
| Déclarations de risques | 22-36/37/38 |
| Déclarations de sécurité | 26-37/39-36 |
| WGK Allemagne | 3 |
| RTECS | CU5760000 |
| Remarque sur les dangers | Irritant |
| TSCA | Oui |
| Code SH | 29124900 |
| Informations MSDS |
| Fournisseur | Langue |
|---|---|
| 3,5-Diméthoxy-4-hydroxybenzaldéhyde | Anglais |
| SigmaAldrich | Anglais |
| ACROS | Anglais |
| ALFA | Anglais |
| Utilisation et synthèse du Syringaldéhyde |
| Aperçu | Le syringaldéhyde est un aldéhyde aromatique prometteur qui ne mérite plus de rester dans l’oubli. Il possède des propriétés bioactives intéressantes et est donc utilisé dans les industries pharmaceutique, alimentaire, cosmétique, textile, des pâtes et papiers, et même dans des applications de contrôle biologique. La forme synthétique du syringaldéhyde est principalement utilisée. Les préoccupations toujours croissantes en matière de sécurité concernant les antioxydants synthétiques et les effets secondaires nocifs des médicaments chimiothérapeutiques, associés à leurs coûts élevés[1], ont ouvert une nouvelle voie pour le développement d’antioxydants, de médicaments et d’additifs alimentaires moins chers, durables et, surtout, naturels.[2]. Le syringaldéhyde, un composé présent seulement en quantité infime dans la nature, est considéré comme une source prometteuse qui répond aux exigences mentionnées ci-dessus. Le syringaldéhyde, ou 3,5-diméthoxy-4-hydroxybenzaldéhyde, est un composé naturel unique doté de caractéristiques bioactives variées qui appartient à la famille des aldéhydes phénoliques. Le syringaldéhyde a une structure très similaire à celle de son fameux homologue, la vanilline, et ses applications sont comparables.[3]. Bien qu'elle ne soit pas aussi bien commercialisée que la vanilline, la chimie du syringaldéhyde et sa manipulation émergent assez rapidement, surtout après la découverte de son rôle d'intermédiaire essentiel des médicaments antibactériens Triméthoprime, Bactrim et Biseptol.[4]. Bactrim ou Biseptol sont des combinaisons de triméthoprime et de sulfaméthoxazole. Ces médicaments sont des bactéricides courants. 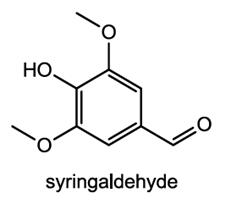 Figure la structure chimique du syringaldéhyde |
| Sources naturelles | Une excellente source naturelle de syringaldéhyde se trouve dans les parois cellulaires des plantes. Étant le deuxième biopolymère le plus abondant après la cellulose, la lignine offre un approvisionnement continu, renouvelable et bon marché en syringaldéhyde. C'est prometteur, puisque la lignine est rejetée comme déchet par l'industrie de la pâte à papier et constitue également un sous-produit majeur du processus de conversion de la biomasse en éthanol.[5]. Malgré le fait que le sort de la lignine se termine dans une raffinerie de biocarburant[6], sa richesse cachée peut être extraite avant sa conversion en matière première biomasse. Bien que cette pratique ne soit pas courante pour la récupération du syringaldéhyde, elle émerge lentement, car les produits à valeur ajoutée issus des déchets offrent un avenir prometteur. Des années de recherches fastidieuses ont conduit au développement et à la compréhension actuels de la synthèse de l’unité syringyle dans les plantes. La lignine étant un hétéropolymère amorphe, l’élucidation de sa voie de biosynthèse n’est pas une tâche facile. Afin d’apprécier la complexité et la diversité de la nature ainsi que ses attributs uniques, il est essentiel de savoir comment l’unité syringyle apparaît dans la lignine. De plus, la bioorigine de ce composé n’a pas été suffisamment étudiée. La composition moléculaire de la protolignine (lignine naturelle) varie d'une plante à l'autre et même d'une cellule à l'autre.[7]. Les recherches ont démontré que les mutants d'Arabidopsis n'étaient plus droits car ils manquaient de fibres interfasciculaires lignifiées, ce qui prouve que la lignine, un macrométabolite, est responsable de l'intégrité structurelle des plantes. La lignine fournit également aux plantes un système vasculaire pour le transport de l'eau et des solutés.[8]. La voie biosynthétique de la protolignine provient principalement de la découverte et de la caractérisation révolutionnaires des enzymes qui conduisent à la synthèse des monolignols des alcools pcoumaryl, coniférylique et sinapylique, par lesquels ils forment les unités hydroxyphényle (H), gaïacyle (G) et syringyle (S). en lignine, respectivement. Ces unités varient structurellement en raison de différents degrés de substituants méthoxy[7]. Les vaisseaux du xylème des plantes sont connus pour fournir à la fois un support mécanique et une conduction de l’eau. Ces vaisseaux sont principalement composés de G-lignine et ne contiennent pas de S-lignine puisque les gènes enzymatiques codant pour l'alcool sinapylique font défaut chez les gymnospermes.[9]. Étant donné que la G-lignine manque dans les angiospermes, des cellules spécialisées supplémentaires, appelées cellules fibreuses, fournissent un soutien mécanique indispensable.[10]. Chose fascinante, chez les angiospermes, ces cellules fibreuses sont principalement composées de S-lignine. Les gènes impliqués dans la synthèse de la lignine S se sont développés bien plus tard que la lignine G, ce qui témoigne de l'évolution des plantes résineuses (gymnospermes) aux plantes feuillues (angiospermes).[11]. De plus, diverses plantes couramment utilisées comme sources de bois et cultures ont été identifiées avec leur teneur en lignine. Ces slignines sont la source à partir de laquelle le syringaldéhyde peut être obtenu lorsque les matériaux lignocellulosiques subissent certaines réactions d'oxydation. |
| Extraction et isolations | Le pourcentage de précurseurs disponibles dans la structure de la lignine détermine strictement la formation de composés phénoliques tels que la vanilline ou le syringaldéhyde. Elle devient plus utile dans la production d'aldéhydes phénoliques lorsque la lignine est soumise à moins de transformations ou de traitements chimiques. Dans une étude utilisant l'oxydation de la lignine, dans laquelle l'influence de l'origine de la lignine, des conditions de production et du type de prétraitement sur les rendements obtenus en vanilline et en syringaldéhyde a été inspectée. Les résultats ont indiqué une compétition entre la condensation des fragments de lignine (fragments syringyle et fragments de gaïacyle) et l'oxydation de la lignine en aldéhydes.[8]. On a obtenu un rendement maximum de 14 % pour les aldéhydes phénoliques totaux (syringaldéhyde + vanilline), basé sur l'oxydation du nitrobenzène en utilisant de la lignine précipitée à partir de liqueur noire kraft avec l'ajout d'un sel de calcium dissous dans de l'alcool soluble dans l'eau. Dans une autre étude, un rendement d'environ 50 à 59,7 % de syringaldéhyde et de vanilline en proportions égales des aldéhydes phénoliques totaux a été obtenu par oxydation du nitrobenzène à partir de la lignine extraite de la paille de riz.[7]. Il a été rapporté que le syringaldéhyde était séparé et analysé via un processus de recristallisation. Une vieille étude[12]a utilisé le processus de recristallisation des produits d'oxydation des tiges de maïs sur l'une des fractions utilisant de l'eau et a obtenu du syringaldéhyde avec un point de fusion signalé de 110 à 112 degrés. Il a également été rapporté que l'oxydation des tiges de maïs produisait des rendements bruts de 3,2 % et un produit de syringaldéhyde pur de 2,6 %. Dans une étude de la composition du syringaldéhyde dans les monocotylédones et dicotylédones d'angiospermes[13], le processus de recristallisation a été utilisé pour purifier le sublimé de syringaldéhyde. Cette étude a rapporté un rendement en aldéhydes phénoliques totaux (vanilline et syringaldéhyde) dans les monocotylédones entre 21 à 30 %, et dans les dicotylédones entre 39 et 48 %. |
| Activité biologique et applications | Les progrès des instruments analytiques, associés aux percées en chimie et en pharmacologie, ont permis l'identification, la quantification et l'isolement des aldéhydes phénoliques pour diverses applications telles que les antioxydants, les agents antifongiques ou antimicrobiens et les agents anti-tumorigenèse dans les produits pharmaceutiques. Dans l’industrie alimentaire, il existe également une tendance à utiliser des composés aromatiques naturels qui présentent des propriétés antioxydantes et antimicrobiennes, fournissant ainsi une source potentielle de conservateurs et d’additifs non synthétiques. Seuls des tests préliminaires in vitro ont été rapportés dans la plupart des cas, mais un nouveau domaine de recherche potentiel et une nouvelle application du syringaldéhyde ont été identifiés. En gardant cela à l’esprit, certaines des propriétés bioactives signalées du syringaldéhyde sont illustrées ici. Capacité antioxydante Une étude relative aux motifs structurels du syringaldéhyde et d'autres benzaldéhydes pour leurs capacités antioxydantes a été abordée par[14]. Dans cette étude, la présence de syringaldéhyde en faibles quantités a montré des résultats impressionnants en matière d’activité de piégeage du peroxyle, sur la base du test CB. Son activité antioxydante a été enregistrée comme étant six fois supérieure à celle de l’aldéhyde protocatéchique. Plus la valeur équivalente Trolox (TEV) est élevée, plus une molécule aura de propriétés antioxydantes. Cette valeur a diminué dans l’ordre suivant : syringaldéhyde > aldéhyde protocatéchique > vanilline. Cette méthode mesure la capacité des molécules dotées de propriétés antioxydantes à supprimer l’ABTS, un chromophore bleu-vert présentant une absorption caractéristique à 734 nm. La capacité de suppression de la molécule est comparée à celle du Trolox, un analogue de la vitamine E. Selon leur étude, la substitution diméthoxy dans le syringaldéhyde ainsi que sa fraction syringol ont été reconnues pour présenter des propriétés antioxydantes améliorées.[14]. Activité antimicrobienne/antifongique Fillat et coll. (2012)[15]ont étudié les effets des phénols de faible poids moléculaire non lixiviables avec lactase sur les fibres de lin non blanchies dans la production de pâtes et papiers biomodifiés. Les chercheurs se concentrent sur l'effet antimicrobien du syringaldéhyde et de l'acétosyringone (un dérivé du syringaldéhyde) dans la réduction de la population de Staphylococcus aureus (Gram+), de Klebsiella pneumonia (Gram-) et de Pseudomonas aeruginosa (Gram-), largement connus pour causer des maladies. chez les humains. La population de pneumonies à Klebsiella a été réduite à 61 % par le syringaldéhyde, tandis que l'acétosyringone a entraîné une réduction importante allant jusqu'à 99 %. Dans le cas de Staphylococcus aureus, la réduction de la population par le syringaldéhyde était de 55 %, soit 15 % de plus que l'acétosyringone. Une autre bactérie, Pseudomonas aeruginosa, a été réduite de 71 % grâce au syringaldéhyde et à un niveau stupéfiant de 97 % grâce à l'acétosyringone. Le rôle du syringaldéhyde en tant qu'agent antifongique contre la levure médicinale Candida guilliermondii semble prometteur. Il a été rapporté que le syringaldéhyde a réussi à inhiber le taux de croissance de C. guilliermondii et à réduire efficacement la production de xylitol. L'effet fongicide est très probablement dû au fragment aldéhyde. Le substituant hydroxyle du syringaldéhyde est soupçonné de jouer un rôle clé dans l’amélioration de cet effet fongicide.[16] Médiateur Le syringaldéhyde a été l'un des premiers médiateurs naturels de laccase découverts. Il a été rapporté qu'il est utilisé comme médiateur dans la dégradation du carmin d'indigo par la laccase bactérienne (oxydoréducase d'oxygène de benzènediol) obtenue à partir de l'organisme -Proteobacterium JB.[18]. L'étude a révélé que le syringaldéhyde était capable d'augmenter la dégradation du carmin d'indigo de 57 %. La dégradation accrue a été rendue possible par les substituants méthyle et méthoxy donneurs d’électrons. Le syringaldéhyde est également utilisé comme médiateur dans les processus de bioblanchiment assistés par laccase. Dans ces processus, des médiateurs synthétiques tels que le HBT, l'acide violurique et la promazine ont été utilisés. Une autre recherche s'est concentrée sur les médiateurs naturels potentiellement rentables dérivés de la lignine, y compris le syringaldéhyde obtenu à partir des liqueurs usées de pâte et des matières végétales utilisées dans le processus de délignification du médiateur-laccase de la pâte à papier en combinaison avec le blanchiment au peroxyde.[17]. Marqueurs organiques dans la fumée de bois Pour confirmer la présence de fractions carbonées dans les émissions de fumée, des biomarqueurs ou des traceurs moléculaires sont utilisés comme indicateurs pour détecter l'origine des produits naturels de la végétation et leurs résidus post-combustion. Des composés phénoliques (comme le syringaldéhyde), obtenus par pyrolyse de la lignine dans la végétation, ont été proposés comme traceurs spécifiques de la taxonomie végétale. Le syringaldéhyde est largement utilisé comme marqueur moléculaire de la fumée de biomasse provenant des particules d'aérosols, notamment pour surveiller les sources de pollution et détecter l'étendue de la combustion.[19]. Étant donné que le changement climatique mondial affecte la fréquence des incendies de forêt, la nécessité d'identifier quantitativement les particules atmosphériques contenues dans la fumée semble revêtir une importance capitale.[20]. Le syringaldéhyde semble jouer un rôle clé dans la détection de la fumée de feuillus. Activité de lutte biologique Le syringaldéhyde a été signalé comme inducteur du gène de virulence d’Agrobacterium tumefaciens. Une étude sur les propriétés insecticides du syringaldéhyde a été réalisée sur des coléoptères Acanthoscelides obtectus.[21]. Le syringaldéhyde a montré une diminution significative de la mobilité naturelle dès le 4ème jour et a provoqué une mortalité significative le 8ème jour. Une enquête utilisant l'analyse spectrophotométrique pour déterminer les acides aminés à l'aide de syringaldéhyde a également été rapportée.[22]. Une méthode spectrophotométrique simple et sensible a été développée pour la détermination cinétique des acides aminés par condensation avec le syringaldéhyde. Cela offre une option supplémentaire dans l’analyse des acides aminés avec des avantages en termes de disponibilité et de stabilité des réactifs et de réduction de la consommation de temps. |
| Les références |
Vergnenegre, A. (2001). Revue des Maladies Respiratoires 18(5), 507-16. Garrote, G. et coll. (2004). Tendances en science et technologie alimentaires 15, 191-200. Bortolomeazzi, R. et al (2001) Chimie alimentaire 100(4), 1481-1489. Rouche, H.-L. (1978). Brevet américain 4 115 650. Xiang, Q. et Lee, Y. (2001). Biochimie appliquée et biotechnologie 91-93(1), 71-80. Kleinert, M. et Barth, T. (2008). Énergie et carburants 22, 13711379. Christiernin, M., et al (2005). Physiologie végétale et biochimie 43(8), 777-785. Hacke, UG et Sperry, JS (2001). Évolution et systématique 4(2), 97-115. Boerjan, W. et coll. (2003). Annuel Rev Plant Biol 54(1), 519-546. Fergus, BJ et coll. (1970). Holzforschung 24(4), 113-117. Li, L. et al (2001) Plant Cell 13(7), 1567-1586. Creighton, RHJ et coll. (1941). JACS 63(1), 312. Creighton, RHJ et coll. (1941). JACS 63(11), 3049-3052. Boundagidou, OG et coll. (2010). Recherche alimentaire internationale 43(8), 2014-2019. Fillat, A. et coll. (2012). Polymères glucidiques 87(1), 146-152. Kelly, C. et coll. (2008). Dans : Biotechnologie pour les carburants et les produits chimiques, Humana Press, 615-626. Camarero, S. et coll. (2007). Technologie enzymatique et microbienne 40(5), 1264-1271. Singh, G. et coll. (2007). Technologie enzymatique et microbienne 41, 794-799. Robinson, AL et coll. (2006). Sciences et technologies environnementales 40(24), 7811-7819 Simoneit, BRT (2002). Géochimie appliquée 17, 129-162. Regnault-Roger, C. et coll. (2004). Journal de recherche sur les produits stockés 40(4), 395-408. Médien, HAA (1998). " Spectrochimica Acta Partie A. : Spectroscopie moléculaire et biomoléculaire, 54(2), 359-365 |
| Propriétés chimiques | poudre cristalline jaune-vert clair à brune |
| Propriétés chimiques | 4-Hydroxy-3,5-diméthoxybenzaldéhyde a une odeur d'alcool |
| Occurrence | Signalé dans l'ananas, la bière, le vin, l'eau-de-vie de raisin, le rhum, de nombreux produits à base de whisky, le sherry, l'orge torréfiée et la fumée de bois dur. |
| Les usages | Le syringaldéhyde est utilisé dans les études biologiques pour l'isolement et la caractérisation structurelle de la lignine du bois moulu, de la lignine dioxane et de la préparation de lignine cellulolytique à partir de drêches de Brewer. |
| Les usages | Le syringaldéhyde peut être utilisé comme étalon de référence analytique pour la détermination de l'analyte dans les extraits de guaco et les préparations pharmaceutiques,(1) les cognacs et les vins,(2) les eaux-de-vie de prune,(4) et la paille de blé(5) par diverses techniques de chromatographie. |
| Préparation | La vanilline est convertie en 5-iodovanilline, qui est traitée avec du méthylate de sodium pour former du 4-hydroxy-3,5- diméthyxybenzaldéhyde. |
| Définition | ChEBI : un hydroxybenzaldéhyde qui est un 4-hydroxybenzaldéhyde substitué par des groupes méthoxy aux positions 3 et 5. Isolé de Pisonia aculeata et Panax japonicus var. majeur, il présente une activité hypoglycémiante. |
| Valeurs seuils d'arôme | Caractéristiques aromatiques à 1,0 % : faiblement sucré, légèrement fumé, cinnamique, vanillé, cuiré avec une nuance médicinale phénolique |
| Référence(s) de synthèse | Revue canadienne de chimie, 31, p. 476, 1953EST CE QUE JE: 10.1139/v53-064 Communications synthétiques, 20, p. 2659, 1990EST CE QUE JE: 10.1080/00397919008051474 |
| Description générale | Le syringaldéhyde est un aldéhyde phénolique aromatique et un produit de dégradation de la lignine. Il présente une activité antioxydante et inhiberait l’enzyme prostaglandine synthétase. La forme synthétique du syringaldéhyde est utilisée commercialement dans les industries pharmaceutique, alimentaire, cosmétique, textile, des pâtes et papiers. |
| Actions Biochimie/Physiol | Odeur à 1,0 % |
| Méthodes de purification | Cristallisez le syringaldéhyde à partir de l’éther animal. [Beilstein 8 H 391, 8 IV 2718.] |
| Produits de préparation et matières premières du Syringaldéhyde |
| Matières premières | Hydrochloric acid-->Pyridine-->Piperidine-->3,4,5-Triméthoxybenzaldéhyde |
| Produits de préparation | BUTYLFORMAMIDE-->3,4-Dimethoxyphenol-->Methyl vanillate-->2,6-Dimethoxyphenol-->2,6-DIMETHOXY-4-METHYLPHENOL-->Ethyl ethoxyacetate-->4-(DIFLUOROMÉTHOXY)-3,5-DIMETHOXYBENZALDEHYDE |
étiquette à chaud: syringaldéhyde, fabricants, fournisseurs, usine de syringaldéhyde en Chine
Vous pourriez aussi aimer
Envoyez demande







