| Description |
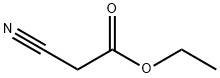
Le cyanoacétate d'éthyle est l'ester éthylique de l'acide cyanoacétique. Le cyanoacétate d'éthyle s'hydrolyse rapidement dans des conditions neutres et alcalines en acide cyanoacétique et en éthanol (et c'est ce qu'il fait dans la plupart des conditions physiologiques et environnementales), tandis qu'à pH acide, la demi-vie est considérablement plus longue.
Une condensation de Knoevenagel du cyanoacétate d'éthyle avec l'aldéhyde est rapportée. Une réaction de condensation de Knoevenegal améliorée par micro-ondes du cyanoacétate d'éthyle avec un aldéhyde, du P2O5, de la pipéridine et du chlorobenzène est rapportée. |
| Propriétés chimiques |
Le cyanoacétate d'éthyle est un liquide incolore à couleur paille avec une odeur douce et agréable. |
| Les usages |
Le cyanoacétate d'éthyle peut être utilisé dans la synthèse du glyoxylate d'éthyle. Il a été utilisé pour étudier les réactions de condensation de Knoevenagel en microréacteur en utilisant des catalyseurs zéolitiques obtenus par greffage de groupes amino sur des zéolites NaX et CsNaX. |
| Les usages |
Réactif utilisé dans la synthèse de pyrimidine et de purine marquée. Le cyanoacétate d'éthyle est un ester. Il peut être utilisé dans la synthèse du glyoxylate d'éthyle. Il a été utilisé pour étudier les réactions de condensation de Knoevenagel en microréacteur en utilisant des catalyseurs zéolitiques obtenus par greffage de groupes amino sur des zéolites NaX et CsNaX. |
| Préparation |
Le cyanoacétate d'éthyle peut être préparé par action du cyanure de sodium ou de potassium sur le chloroacétate d'éthyle et par action du cyanure de sodium sur le chloroacétate de sodium, suivie d'une estérification. |
| Description générale |
Un liquide incolore. Plus dense que l'eau. Le contact peut irriter la peau, les yeux et les muqueuses. Point d'éclair 210 degrés F. Peut être toxique par ingestion. Utilisé pour fabriquer d’autres produits chimiques. |
| Réactions à l'air et à l'eau |
Légèrement soluble dans l'eau. |
| Profil de réactivité |
Le cyanoacétate d'éthyle est à la fois un nitrile et un ester. Les esters réagissent avec les acides pour libérer de la chaleur avec les alcools et les acides. Les acides oxydants forts peuvent provoquer une réaction vigoureuse suffisamment exothermique pour enflammer les produits de réaction. La chaleur est également générée par l'interaction des esters avec des solutions caustiques. L'hydrogène inflammable est généré en mélangeant des esters avec des métaux alcalins et des hydrures. Les nitriles peuvent polymériser en présence de métaux et de certains composés métalliques. Ils sont incompatibles avec les acides ; le mélange de nitriles avec des acides oxydants forts peut conduire à des réactions extrêmement violentes. Les nitriles sont généralement incompatibles avec d'autres agents oxydants tels que les peroxydes et les époxydes. La combinaison de bases et de nitriles peut produire du cyanure d'hydrogène. Les nitriles sont hydrolysés à la fois dans un acide et une base aqueux pour donner des acides carboxyliques (ou des sels d'acides carboxyliques). Ces réactions génèrent de la chaleur. Les peroxydes convertissent les nitriles en amides. Les nitriles peuvent réagir vigoureusement avec les agents réducteurs. L'acétonitrile et le propionitrile sont solubles dans l'eau, mais les nitriles supérieurs au propionitrile ont une faible solubilité aqueuse. Ils sont également insolubles dans les acides aqueux. |
| Danger |
Toxique par ingestion et inhalation. |
| Danger pour la santé |
TOXIQUE; l'inhalation, l'ingestion ou le contact (peau, yeux) avec des vapeurs, des poussières ou une substance peut provoquer des blessures graves, des brûlures ou la mort. Le contact avec la substance fondue peut provoquer de graves brûlures à la peau et aux yeux. La réaction avec l'eau ou l'air humide dégagera des gaz toxiques, corrosifs ou inflammables. La réaction avec l'eau peut générer beaucoup de chaleur qui augmentera la concentration de fumées dans l'air. Le feu produira des gaz irritants, corrosifs et/ou toxiques. Le ruissellement des eaux de lutte contre les incendies ou de dilution peut être corrosif et/ou toxique et provoquer une pollution. |
| Risque d'incendie |
Matière combustible : peut brûler mais ne s'enflamme pas facilement. La substance réagira avec l'eau (certaines violemment) en libérant des gaz et un ruissellement inflammables, toxiques ou corrosifs. Lorsqu'elles sont chauffées, les vapeurs peuvent former des mélanges explosifs avec l'air : risques d'explosion à l'intérieur, à l'extérieur et dans les égouts. La plupart des vapeurs sont plus lourdes que l'air. Ils se propagent sur le sol et s'accumulent dans les zones basses ou confinées (égouts, sous-sols, réservoirs). Les vapeurs peuvent se déplacer vers une source d'inflammation et provoquer un retour de flamme. Le contact avec des métaux peut dégager de l'hydrogène gazeux inflammable. Les conteneurs peuvent exploser lorsqu'ils sont chauffés ou s'ils sont contaminés par de l'eau. |
| Profil de sécurité |
intoxication par ingestion. Modérément toxique par voies intrapéritonéale et sous-cutanée. Combustible lorsqu'il est exposé à la chaleur ou aux flammes ; peut réagir avec des matières comburantes. Wdl réagit avec l'eau ou la vapeur pour produire des vapeurs toxiques et inflammables. Pour lutter contre l'incendie, utilisez du CO2, de la poudre chimique. Lorsqu'il est chauffé jusqu'à décomposition ou au contact d'un acide ou de vapeurs acides, il émet des fumées hautement toxiques de CN-. Voir aussi NITRILES. |
| Exposition potentielle |
Un nitrile utilisé pour fabriquer des colorants, des produits pharmaceutiques et d'autres produits chimiques. |
| PREMIERS SECOURS |
Si ce produit chimique entre en contact avec les yeux, retirez immédiatement toutes les lentilles de contact et irriguez immédiatement pendant au moins 15 minutes, en soulevant de temps en temps les paupières supérieures et inférieures. Consultez immédiatement un médecin. Si ce produit chimique entre en contact avec la peau, retirez les vêtements contaminés et lavez-les immédiatement avec de l'eau et du savon. Consultez immédiatement un médecin. Si ce produit chimique a été inhalé, retirer du lieu d'exposition, commencer la respiration artificielle (en utilisant les précautions universelles, y compris un masque de réanimation) si la respiration s'est arrêtée et la RCR si l'action cardiaque s'est arrêtée. Transférer rapidement vers un établissement médical. Lorsque ce produit chimique a été avalé, consultez un médecin. Donner de grandes quantités d'eau et faire vomir. Ne pas faire vomir une personne inconsciente |
| stockage |
emplacement du poison. Avant de travailler avec ce produit chimique, vous devez être formé à sa manipulation et à son stockage appropriés. Conserver dans des récipients bien fermés dans un endroit frais et bien ventilé, à l'écart des oxydants, des bases fortes, des acides forts, des agents réducteurs, de l'humidité et des sources d'inflammation. Dans la mesure du possible, pompez automatiquement le liquide des fûts ou autres conteneurs de stockage vers les conteneurs de traitement. |
| Expédition |
UN3276 Nitriles liquides, toxiques, nsa, classe de danger : 6.1 ; Étiquettes : 6.1-Matériaux toxiques, nom technique requis, risque potentiel d'inhalation (disposition spéciale 5). |
| Méthodes de purification |
Secouez l'ester plusieurs fois avec du Na2CO3 aqueux à 10 %, lavez-le bien avec de l'eau, séchez-le avec du Na2SO4 et distillez-le de manière fractionnée. [Beilstein 2 IV 1889.] |
| Incompatibilités |
Incompatible avec les oxydants (chlorates, nitrates, peroxydes, permanganates, perchlorates, chlore, brome, fluor, etc.) ; tout contact peut provoquer des incendies ou des explosions. Tenir à l’écart des matières alcalines, des bases fortes, des acides forts, des oxoacides, des époxydes et des agents réducteurs. Les nitriles peuvent polymériser en présence de métaux et de certains composés métalliques. Ils sont incompatibles avec les acides ; le mélange de nitriles avec des acides oxydants forts peut conduire à des réactions extrêmement violentes. Les nitriles sont généralement incompatibles avec d'autres agents oxydants tels que les peroxydes et les époxydes. La combinaison de bases et de nitriles peut produire du cyanure d'hydrogène. Les nitriles sont hydrolysés à la fois dans un acide et une base aqueux pour donner des acides carboxyliques (ou des sels d'acides carboxyliques). Ces réactions génèrent de la chaleur. Les peroxydes convertissent les nitriles en amides. Les nitriles peuvent réagir vigoureusement avec les agents réducteurs. L'acétonitrile et le propionitrile sont solubles dans l'eau, mais les nitriles supérieurs au propionitrile ont une faible solubilité aqueuse. Ils sont également insolubles dans les acides aqueux. Réagit avec l'humidité, l'eau et la vapeur, formant des fumées toxiques. |
| Traitement des déchets |
Consulter les agences de réglementation environnementale pour obtenir des conseils sur les pratiques d'élimination acceptables. Les générateurs de déchets contenant ce contaminant (supérieur ou égal à 100 kg/mois) doivent se conformer aux réglementations de l'EPA régissant le stockage, le transport, le traitement et l'élimination des déchets. |