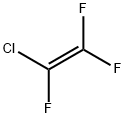
| Propriétés chimiques |
Gaz incolore; légère odeur éthérée. Se décompose dans l'eau. |
| Utilisations |
Intermédiaire, monomère pour résines chlorotrifluoroéthylène. |
| Préparation |
Le chlorotrifluoroéthylène est préparé à partir de l'éthylène par la voie suivante : 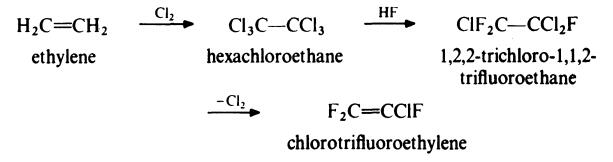
L'éthylène est traité avec un excès de chlore à 300-350??C en présence de charbon actif pour donner de l'hexachloroéthane. Ce produit est ensuite traité avec du fluorure d'hydrogène en présence de pentachlorure d'antimoine pour donner du trichlorotrifluoroéthane. La déchloration en phase liquide avec de la poussière de zinc et de l'éthanol conduit à la formation de chlorotrifluoroéthylène qui est lavé à l'eau pour éliminer l'alcool, séché et distillé sous pression. |
| Référence(s) de synthèse |
Journal de chimie organique, 57, p. 5018, 1992DOI:10.1021/jo00044a044 |
| Description générale |
Le chlorotrifluoroéthylène est un gaz incolore à l'odeur légèrement éthérée. Il est expédié sous forme de gaz liquéfié sous sa pression de vapeur. Le chlorotrifluoroéthylène est très toxique par inhalation et s'enflamme facilement. Les vapeurs sont plus lourdes que l'air et une flamme peut facilement revenir à la source de la fuite. Cette fuite peut être une fuite de liquide ou de vapeur. Les vapeurs peuvent s'asphyxier par le déplacement de l'air. Le contact avec le liquide peut provoquer des engelures. En cas d'exposition prolongée à une chaleur intense ou à un incendie, les conteneurs peuvent se rompre violemment et exploser, ou le matériau peut se polymériser et risquer de se rompre. |
| Réactions de l'air et de l'eau |
Hautement inflammable. |
| Profil de réactivité |
Les composés aliphatiques halogénés, comme le chlorotrifluoroéthylène, sont moyennement ou très réactifs. La réactivité diminue généralement avec l'augmentation du degré de substitution des atomes d'hydrogène par des halogènes. Les haloalcanes de faible poids moléculaire sont hautement inflammables et peuvent réagir avec certains métaux pour former des produits dangereux. Les matériaux de ce groupe sont incompatibles avec les agents oxydants et réducteurs puissants. Ils sont également incompatibles avec de nombreuses amines, nitrures, composés azoïques/diazoïques, métaux alcalins, oxydants puissants tels que le perchlorate de chlore, l'oxygène, le brome et les époxydes. |
| Danger |
Risque d'incendie dangereux. Limites d'inflammabilité dans l'air 8,4–38,7 %. |
| Danger pour la santé |
L'inhalation provoque des étourdissements, des nausées, des vomissements ; des lésions hépatiques et rénales peuvent se développer après plusieurs heures et provoquer une jaunisse et une nécrose des reins. Le contact avec le liquide provoque des engelures des yeux et éventuellement de la peau. |
| Inflammabilité et explosibilité |
Extrêmement inflammable |
| Profil de sécurité |
Toxique par ingestion et par voie intrapéritonéale. Modérément toxique par inhalation. Risque d'incendie très dangereux en cas d'exposition à la chaleur, aux flammes (étincelles) ou aux oxydants. Pour combattre l'incendie, arrêter le débit de gaz. Réaction violente en cas de mélange avec (Brz + 02) ou (CIF3 + eau). Réaction de polymérisation potentiellement explosive avec l'éthylène. Incompatible avec le 1,1-dchloroéthylène ; l'oxygène. Lorsqu'il est chauffé jusqu'à décomposition, il émet des fumées toxiques de F et Cl-. Voir également HYDROCARBURES CHLORÉS, ALIPHATIQUES ; et FLUORURES. |
| Méthodes de purification |
Frotter avec une solution de KOH à 10 %, puis avec une solution de H2SO4 à 10 % pour éliminer les inhibiteurs, sécher et passer au gel de silice. Il est stabilisé avec environ 1 % de tributylamine. Utiliser un équipement en laiton. [Beilstein 1 III 646.] GAZ TOXIQUE. |