
Présentation du produit
| Fluorocytosine Informations de base |
| Présentation Mécanisme d'action et résistance Pharmacocinétique et posologie Toxicité et effets secondaires Références |
| Nom du produit : | Fluorocytosine |
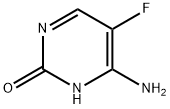
| Synonymes : | 4-amino-5-fluoro-2(1h)-pyrimidinone ;4-Amino-5-fluoro-2(1H)-pyrmidinone ;{{10} }fluorocystosine;5-fluorocytosine;5-fluoro-cytosine;fluocytosine;4-Amino-5-Fluoro-2(1H)-pyrimidine, Flucytosine, {{19} }FC ;5-Fluorocytosine 98 % |
| CAS : | 2022-85-7 |
| MF : | C4H4FN3O |
| MO : | 129.09 |
| EINECS : | 217-968-7 |
| Catégories de produits: | Nucléotides et nucléosides ; Antifongiques pour la recherche et l'utilisation expérimentale ; Biochimie ; Réactifs chimiques pour la recherche en pharmacologie ; Nucléobases et leurs analogues ; Nucléosides, nucléotides et réactifs associés ; Série pyrimidine ; Acide phénylacétique ; cétone ; Acides nucléiques ; Bases et réactifs associés ; Nucléotides ; Amines ;Hétérocycles;PYRIMIDINE;Pyridines, Pyrimidines, Purines et Ptérines;API;amine |cétone| Fluor d'alkyle ; GLUCOTROL ; Anticancer ;2022-85-7 |
| Fichier Mol : | 2022-85-7.mol |
 |
|
| Propriétés chimiques de la fluorocytosine |
| Point de fusion | 298-300 degré (déc.) (lit.) |
| densité | 1,3990 (estimation) |
| la pression de vapeur | 0Pa à 25 degrés |
| température de stockage. | 2-8 diplôme |
| solubilité | Peu soluble dans l'eau, légèrement soluble dans l'éthanol (96 %) |
| formulaire | Poudre cristalline |
| Le PKA | 3,26 (à 25 degrés) |
| couleur | Blanc à presque blanc |
| Solubilité dans l'eau | 1,5 g/100 ml (25 ºC) |
| Sensible | Sensible à la lumière |
| Merck | 14,4125 |
| BRN | 127285 |
| Classe BCS | 1 |
| La stabilité: | Sensible à la lumière |
| InChIKey | XRECZIEBJDKEO-UHFFFAOYSA-N |
| Connexion | -1.36 à 22,1 degrés et pH6.4-6.9 |
| Constante de dissociation | 2.74-10.71 à 21,4 degrés |
| Référence de la base de données CAS | 2022-85-7(Référence de la base de données CAS) |
| Information de sécurité |
| Codes de danger | Xn,T,Xi |
| Déclarations de risques | 40-36/37/38-63 |
| Déclarations de sécurité | 22-24/25-45-36/37-36/37/39-27-26 |
| WGK Allemagne | 2 |
| RTECS | HA6040000 |
| F | 10-23 |
| Remarque sur les dangers | Toxique/sensible à la lumière |
| Classe de danger | IRRITANT, SENSIBLE À LA LUMIÈRE |
| Code SH | 29335990 |
| Données sur les substances dangereuses | 2022-85-7(Données sur les substances dangereuses) |
| Toxicité | LD50 in mice (mg/kg): >2000 oralement et sc; 1190 IP ; 500 iv (Grunberg, 1963) |
| Informations MSDS |
| Fournisseur | Langue |
|---|---|
| 2-Hydroxy-4-amino-5-fluoropyrimidine | Anglais |
| SigmaAldrich | Anglais |
| ACROS | Anglais |
| ALFA | Anglais |
| Utilisation et synthèse de la fluorocytosine |
| Aperçu | Une pyrimidine fluorée, la 5-flucytosine (fluorocytosine ; 5-FC, Fig. 1), a été initialement développée comme agent anticancéreux potentiel, mais elle n'a pas été suffisamment efficace dans le domaine de la chimiothérapie anticancéreuse.[1]. Plus tard, 5-FC s'est révélé actif dans la candidose expérimentale et la cryptococcose chez la souris.[2]et a été utilisé pour traiter les infections humaines[3]. En plus de son activité contre Candida et Cryptococcus, 5-FC a également une activité inhibitrice contre les champignons responsables de la chromoblastomycose.[4]; cependant, il est inefficace contre les infections causées par des champignons filamenteux. 5-FC a une forte prévalence de résistance primaire chez de nombreuses espèces fongiques. En raison de cette résistance primaire, le 5-FC est principalement utilisé en association avec d'autres antifongiques (principalement l'amphotéricine B, AmB) et plus récemment, il a été étudié en association avec d'autres agents, notamment le fluconazole (FLU), le kétoconazole (KTZ), l'itraconazole (ITRA), le voriconazole (VORI) et les échinocandines (par exemple, micafungine, MICA et caspofungine, CAS). Il n’est que rarement utilisé en monothérapie. La flucytosine (5-FC) est un composé antimycosique synthétique, synthétisé pour la première fois en 1957. Il n'a aucune capacité antifongique intrinsèque, mais après avoir été absorbé par les cellules fongiques sensibles, il est converti en 5-fluorouracile ( 5-FU), qui est ensuite converti en métabolites qui inhibent la synthèse fongique de l'ARN et de l'ADN. La monothérapie avec 5-FC est limitée en raison du développement fréquent de résistances. En association avec l'amphotéricine B, le 5-FC peut être utilisé pour traiter les mycoses systémiques graves, telles que la cryptococcose, la candidose, la chromoblastomycose et l'aspergillose. 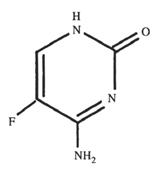 Figure 1 la structure chimique de la Fluorocytosine |
| Mécanisme d'action et de résistance | 5-FC est particulièrement actif contre les levures, notamment Candida, Torulopsis et Cryptococcus spp., ainsi que contre les champignons dématiacés responsables de la chromomycose (Phialophora et Cladosporium spp.) et Aspergillus spp.[5]Les CMI de {{0}}FC varient de 0,1 à 0,25 mg/L pour ces espèces fongiques. Chez Emmonsia crescens, Emmonsia parva, Madurella mycetomatis, Madurella grisea, Pyrenochaeta romeroi, Cephalosporium spp., Sporothrix schenckii et Blastomyces dermatitidis, les CMI varient de 100 à 1 000 mg/L.14 5-FC est également actif contre certains protozoaires, notamment Acanthamoeba culbertsoni in vitro et in vivo et Leishmania spp. chez les patients.[5] L'activité antimycotique du 5-FC résulte de sa conversion rapide en 5-fluorouracile (5-FU) par l'enzyme cytosine désaminase, dans les cellules fongiques sensibles. Il existe deux mécanismes impliqués par lesquels le 5-fluorouracile exerce son activité antifongique. Le premier mécanisme comprend la conversion du 5-fluorouracile via le 5-monophosphate de fluoruridine (FUMP) et le 5-diphosphate de fluoruridine (FUDP) en 5-triphosphate de fluoruridine (FUTP)[6]. Le FUTP est en outre incorporé dans l'ARN fongique à la place de l'acide uridylique ; cela modifie l'aminoacylation de l'ARNt, perturbe le pool d'acides aminés et inhibe la synthèse des protéines[6]. Le deuxième mécanisme est le métabolisme du 5-FU en 5-fluorodésoxyuridine monophosphate (FdUMP) par l'uridine monophosphate pyrophosphorylase.[6]. FdUMP est un puissant inhibiteur de la thymidylate synthase, une enzyme clé impliquée dans la synthèse de l'ADN et la division nucléaire.[7]. Ainsi, 5-FC agit en interférant avec le métabolisme de la pyrimidine et la synthèse des protéines dans la cellule fongique. Cette activité entraîne la lyse et la mort des cellules. L'apparition d'une résistance lors de l'utilisation du 5-FC a été largement décrite et exclut l'utilisation du 5-FC en monothérapie.[8, 10]Deux mécanismes fondamentaux de résistance peuvent être distingués : (i) certaines mutations peuvent entraîner un déficit des enzymes nécessaires au transport cellulaire et à l'absorption du 5-FC ou à son métabolisme (c'est-à-dire la cytosine perméase, l'uridine monophosphate pyrophosphorylase ou la cytosine désaminase );[9,11](ii) la résistance peut résulter d'une synthèse accrue de pyrimidines, qui entrent en compétition avec les antimétabolites fluorés du 5-FC et diminuent ainsi son activité antimycotique.[9]Il a été démontré que l'uridine monophosphate pyrophosphorylase défectueuse est le type le plus fréquent de résistance acquise au 5-FC dans les cellules fongiques.[12]Normark & Schönebeck ont signalé que deux phénotypes différents de souches 5-résistantes au FC peuvent être reconnus :[10]les souches de phénotype de résistance classe 1 ne sont pas affectées par le 5-FC à des concentrations élevées (ce sont les souches totalement (intrinsèquement) résistantes), tandis que celles de classe 2 sont sensibles au 5-FC à de faibles concentrations mais, après une longue exposition au 5-FC (même à des concentrations élevées), une résistance se développe (on dit que ceux-ci sont partiellement résistants ou ont acquis une résistance). Le développement de résistances chez ces dernières souches résulte probablement de la sélection de mutants non sensibles, conduisant à une population résistante secondaire.[9] L'incidence de la résistance au 5-FC varie selon les espèces.20 Jusqu'à 7 à 8 % des souches intrinsèquement résistantes se trouvent parmi les isolats de prétraitement de C. albicans, de candida non spécifié et de Torulopsis glabrata. Chez C. neoformans, l'incidence de la résistance est plus faible (1 à 2 %), mais chez Candida spp. hormis C. albicans, il est de 22 %, en raison de la prévalence d'espèces généralement moins sensibles telles que Candida tropicalis et Candida krusei.[13]. L’incidence exacte de la résistance primaire au 5-FC n’est pas claire. Différents enquêteurs rapportent des taux compris entre 8 % et 44 % pour Candida spp.[14]. Les facteurs possibles contribuant à cette large gamme comprennent les méthodes de sensibilité utilisées, les facteurs locaux impliquant l'utilisation d'agents antifongiques et les différences dans la prévalence de diverses espèces de Candida.[14]. |
| Pharmacocinétique et posologie | 5-Le FC est absorbé très rapidement et presque complètement : 76 à 89 % sont biodisponibles après administration orale.[16]Chez les patients ayant une fonction rénale normale, les concentrations maximales sont atteintes dans le sérum et d'autres liquides organiques en 1 à 2 heures.[15, 16]. 5-Le FC pénètre bien dans la plupart des sites corporels, y compris les liquides céphalo-rachidiens, vitré et péritonéal, ainsi que dans les articulations enflammées, car il est petit et hautement soluble dans l'eau et n'est pas fortement lié aux protéines sériques.[15-17]. 5-Le FC est principalement éliminé par les reins et la clairance plasmatique du médicament est étroitement liée à la clairance de la créatinine.[15, 17]. 5-Le FC n'est que peu métabolisé dans le foie. L'élimination rénale se fait par filtration glomérulaire ; aucune résorption ou sécrétion tubulaire n'a lieu. La demi-vie du 5-FC est d'environ 3 à 4 heures chez les patients ayant une fonction rénale normale, mais peut être prolongée jusqu'à 85 heures chez les patients présentant une insuffisance rénale sévère.[12, 16, 18]L'insuffisance rénale modifie la pharmacocinétique de la 5-FC car elle ralentit l'absorption, prolonge la demi-vie sérique et diminue la clairance.[15]. Le volume apparent de distribution de 5-FC se rapproche de celui de l'eau corporelle totale et n'est pas modifié par l'insuffisance rénale. La posologie doit être adaptée chez les patients présentant une insuffisance rénale. Diverses recommandations ont été faites[15-18]. Daneshmend & Warnock ont suggéré les directives suivantes pour l'administration de 5-FC aux patients souffrant d'insuffisance rénale.[15]. In patients with a creatinine clearance of >40 mL/min, une dose standard de 37,5 mg/kg toutes les 6 heures doit être utilisée. Si la clairance de la créatinine est comprise entre 20 et 40 mL/min, la dose recommandée est de 37,5 mg/kg toutes les 12 h. Chez les patients présentant une clairance de la créatinine de<20 mL/ minute, the dose of 5-FC should be 37.5 mg/kg once daily. Finally, if the creatinine clearance is <10 mL/min, frequent determinations of 5-FC concentration should be used as guidance for the frequency of dosing. |
| Toxicité et effets secondaires | 5-Le FC est connu pour avoir des effets secondaires relativement mineurs, tels que des nausées, des vomissements et de la diarrhée, mais il a également des effets secondaires plus graves, notamment une hépatotoxicité et une dépression médullaire. Les effets secondaires gastro-intestinaux, les effets secondaires les plus courants et les moins nocifs associés au traitement 5-FC, comprennent les nausées, la diarrhée et, occasionnellement, les vomissements et les douleurs abdominales diffuses. Ils surviennent chez environ 6 % des patients traités par 5-FC[18]. Bien que ces effets secondaires ne soient généralement pas graves ; deux cas de colite ulcéreuse et de perforation intestinale ont été rapportés[19]. Une hépatotoxicité peut survenir pendant le traitement 5-FC. Dans la plupart des cas, il s’agit d’une augmentation des concentrations sériques de transaminases et de phosphatase alcaline.[20]. L'incidence de l'hépatotoxicité est comprise entre 0 et 25 %[20]. La toxicité la plus grave associée au traitement 5-FC est la dépression médullaire. Plusieurs cas de leucocytopénie, de thrombocytopénie et/ou de pancytopénie graves ou potentiellement mortelles ont été rapportés.[21-23]. Le mécanisme de toxicité du 5-FC n'est pas encore entièrement compris. Il est probable que certains des effets secondaires provoqués par le 5-FC, par exemple l'hépatotoxicité et la dépression médullaire, dépendent de la dose, bien que tous les rapports ne soutiennent pas cette théorie. De plus, il a été postulé que la conversion du 5-FC en certains métabolites, notamment le 5-FU, pourrait être l'un des mécanismes de développement de la toxicité associée au 5-FC. |
| Les références |
Heidelberg C, Chaudhuri NK, Danneberg P et al. Pyrimidines fluorées, une nouvelle classe de composés inhibiteurs de tumeurs. Nature 1957 ; 179 (4561) : 663-666 Grunberg E, Titsworth E, Bennett M. Activité chimiothérapeutique de la 5-fluorocytosine. Agents antimicrobiens Chemother 1963 ; 161 : 566-568 Gland D, Madoff MA. Traitement de la septicémie à Candida et de la méningite à Cryptococcus avec la 5-fluorocytosine. Un nouvel agent antifongique. JAMA 1968 ; 206(4) : 830-832 Benson JM, Nahata MC. Utilisation clinique d'agents antifongiques systémiques. ClinPharm 1988 ; 7(6) : 424-438 Scholer, HJ (1980). Flucytosine. Dans Chimiothérapie antifongique, (Speller, DCE, Ed.), pp. 35-106. Wiley, Chichester. Waldorf AR, Polak A. Mécanismes d'action de la 5-fluorocytosine. Agents antimicrobiens Chemother 1983 ; 23(1):79-85 Diasio RB, Bennett JE, Myers CE. Mode d'action de la 5-fluorocytosine. Biochem Pharmacol 1978; 27(5):703-707 Polak, A. et Scholer, HJ (1975). Mode d'action de la 5-fluorocytosine et mécanismes de résistance. Chimiothérapie 21, 113-30. Polak, A. (1977). 5-État actuel de la fluorocytosine avec des références spéciales au mode d'action et à la résistance aux médicaments. Contributions à la microbiologie et à l'immunologie 4, 158-67. Normark, S. et Schönebeck, J. (1973). Études in vitro de la résistance à la 5-fluorocytosine chez Candida albicans et Torulopsis glabrata. Agents antimicrobiens et chimiothérapie 2, 114-21. Fasoli, M. et Kerridge, D. (1988). Isolement et caractérisation de mutants résistants à la fluoropyrimidine chez deux espèces de Candida. Annales de l'Académie des sciences de New York 544, 260-3. Francis, P. et Walsh, TJ (1992). Rôle évolutif de la flucytosine chez les patients immunodéprimés : nouvelles connaissances sur la sécurité, la pharmacocinétique et le traitement antifongique. Maladies infectieuses cliniques 15, 1003–18. Medoff, G. et Kobayashi, GS (1980). Stratégies de traitement des infections fongiques systémiques. Journal de médecine de la Nouvelle-Angleterre 302, 145-55. Armstrong, D. et Schmitt, HJ (1990). Médicaments plus anciens. Dans Chimiothérapie pour les maladies fongiques, (Ryley, JF, Ed.), pp. 439-54. Springer-Verlag, Berlin. Daneshmend, TK et Warnock, DW (1983). Pharmacocinétique clinique des médicaments antifongiques systémiques. Pharmacocinétique clinique 8, 17–42. Cutler, RE, Blair, AD et Kelly, MR (1978). Cinétique de la flucytosine chez les sujets présentant une fonction rénale normale ou altérée. Pharmacologie clinique et thérapeutique 24, 333-42. Block, ER, Bennett, JE, Livoti, LG, Klein, WJ, MacGregor, RR et Henderson, L. (1974). Flucytosine et amphotéricine B : effets de l'hémodialyse sur la concentration plasmatique et la clairance. Etudes chez l'homme. Annales de médecine interne 80, 613-7. Schönebeck, J., Polak, A., Fernex, M. et Scholer, HJ (1973). Études pharmacocinétiques sur l'agent antimycotique oral 5-fluorocytosine chez des personnes ayant une fonction rénale normale ou altérée. Chimiothérapie 18, 321-36. Benson, JM et Nahata, MC (1988). Utilisation clinique d'agents antifongiques systémiques. Pharmacie clinique 7, 424-38. Bennet, JE (1977). Flucytosine. Annales de médecine interne 86, 319-21. Kauffman, CA et Frame, PT (1977). Toxicité médullaire associée au traitement à la 5-fluorocytosine. Agents antimicrobiens et chimiothérapie 11, 244–7. Schlegel, RJ, Bernier, GM, Bellanti, JA, Maybee, DA, Osborne, GB, Stewart, JL et al. (1970). Candidose sévère associée à une dysplasie thymique, un déficit en IgA et des effets antilymphocytaires plasmatiques. Pédiatrie 45, 926-936. Meyer, R. et Axelrod, JL (1974). Anémie aplasique mortelle résultant de la flucytosine. Journal de l'Association médicale américaine 228, 1573. |
| Description | La 5-Fluorocytosine (5-FC), un analogue de la pyrimidine fluorée, est un promédicament antimycotique synthétique qui est converti par la cytosine désaminase en 5-fluorouracile. 5-Le fluorouracile, un médicament cytotoxique largement utilisé, est ensuite métabolisé en ribo- et désoxyribonucléotides fluorés, entraînant l'inhibition de la synthèse de l'ADN et des protéines, ce qui a de multiples effets, notamment l'inhibition deCandidoseespèces etC. néoformiensinfections et cytotoxicité envers les cellules cancéreuses. En combinaison avec un vecteur de réplication rétroviral portant un gène activant un promédicament de la cytosine désaminase, il a été démontré que le 5-FC élimine sélectivement les cellules tumorales CT26 et Tu-2449.in vitro(CI50s=4,2 et 1,5 μM, respectivement) et pour améliorer significativement la survie et réduire la taille de la tumeur (à une dose de 500 mg/kg) dans deux modèles différents de gliomes syngéniques de souris. |
| Propriétés chimiques | Solide cristallin blanc |
| Auteur | Ancobon,Roche,États-Unis,1972 |
| Les usages | 5-FC est un agent antifongique/antimicrobien toxique |
| Les usages | 5-La fluorocytosine agit comme un agent antidiabétique, antifongique et antimicrobien. Il est utile pour le traitement des infections graves dues à des souches sensibles de Candida ou Cryptococcus neoformans et à la chromomycose. De plus, il est utilisé dans des études sur la biosynthèse du TMP. |
| Définition | ChEBI : La flucytosine est un composé organofluoré qui est une cytosine substituée en position 5 par un fluor. Promédicament de l'antifongique 5-fluorouracile, il est utilisé pour le traitement des infections fongiques systémiques. Il a un rôle de promédicament. C'est un composé organofluoré, une pyrimidone, une aminopyrimidine, un analogue nucléosidique et un médicament antifongique pyrimidine. Il est fonctionnellement lié à une cytosine. |
| Les indications | La flucytosine (Ancobon) est une pyrimidine synthétique fluorée dont la structure est apparentée au fluorouracile (FU) et à la floxuridine. Il peut être fongistatique et fongicide. Bien qu'il soit utilisé plus fréquemment dans le traitement des infections systémiques causées par Candida et Cryptococcus, les indications dermatologiques peuvent inclure des infections dues à la chromomycose, à la sporotrichose, aux espèces Cladosporium et Sporothrix. Il est généralement inefficace contre les espèces Aspergillus. |
| Processus de fabrication | La préparation du 5-fluorouracile est indiquée sous « Fluorouracile ». Comme décrit dans le brevet américain 3 040 026, le 5-fluorouracile est ensuite soumis aux étapes suivantes pour donner de la flucytosine. Étape 1 : 2,4-Dichloro-5-Fluoropyrimidine - Un mélange de 104 grammes (0,8 mol) de 5-fluorouracile, 1 472 grammes (9,6 moles) d'oxychlorure de phosphore et 166 grammes (1,37 moles) de diméthylaniline ont été agités au reflux pendant 2 heures. Après refroidissement à température ambiante, l'oxychlorure de phosphore a été éliminé par distillation entre 18 et 22 mm et entre 22 et 37 degrés. Le résidu a ensuite été versé dans un mélange vigoureusement agité de 500 ml d'éther et 500 grammes de glace. Après séparation de la couche d'éther, la couche aqueuse a été extraite avec 500 ml, puis 200 ml d'éther. Les fractions d'éther combinées ont été séchées sur sulfate de sodium, filtrées et l'éther éliminé par distillation sous vide entre 10 et 22 degrés. Le résidu, un solide jaune fondant entre 37 et 38 degrés, pesait 120 grammes correspondant à un rendement de 90 %. La distillation sous vide de 115 grammes de ce matériau entre 74 et 80 degrés (16 mm) a donné 108 grammes de solide blanc fondant entre 38 et 39 degrés, correspondant à un rendement de 84,5 %. Étape 2 : 2-Chloro-4-Amino-5-Fluoropyrimidine - Pour une solution de 10.0 grammes (0.{{27} }6 mol) de 2,4-dichloro-5-fluoropyrimidine dans 100 ml d'éthanol, 25 ml d'ammoniaque concentrée ont été ajoutés lentement. Il en résulte une solution légèrement opalescente. La température est montée progressivement jusqu'à 35 degrés. La solution a ensuite été refroidie dans la glace à 18 degrés et est ensuite restée en dessous de 30 degrés. Au bout de trois heures, un titrage Volhard montre que 0,0545 mole de chlore est présente sous forme ionique. Le stockage au réfrigérateur pendant la nuit a entraîné une certaine cristallisation du chlorure d'ammonium. Une boue blanche, résultant de l'évaporation du mélange réactionnel à 40 degrés, a été mise en suspension avec 75 ml d'eau, filtrée et lavée pour éliminer tout chlorure. Après séchage sous vide, le produit a fondu entre 196,5 degrés et 197,5 degrés, donnant 6,44 grammes. L'évaporation des liqueurs mères a donné une deuxième récolte de 0,38 gramme, portant le rendement total à 6,82 grammes (79,3 %). Étape 3 : 5-Fluorocytosine - Une bouillie de 34,0 grammes (0,231 mol) de 2-chloro-4- amino-5-fluoropyrimidine dans 231 ml d'acide chlorhydrique concentré, on a chauffé dans un bain-marie entre 93 et 95 degrés pendant 125 minutes. La réaction a été suivie par spectrophotométrie ultraviolette en utilisant l'absorption à 245, 285 et 300 mμ comme guide. L'absorption à 300 mμ a atteint un maximum après 120 minutes puis a légèrement diminué. La solution claire a été refroidie à 25 degrés dans un bain de glace, puis évaporée à sec sous vide à 40 degrés. Après mise en suspension avec de l'eau trois fois et réévaporation, le résidu a été dissous dans 100 millilitres d'eau. A cette solution refroidie dans la glace, 29 ml d'ammoniaque concentrée ont été ajoutés goutte à goutte. Le précipité résultant a été filtré, lavé du chlorure avec de l'eau, puis avec de l'alcool et de l'éther. Après séchage sous vide à 65 degrés, le produit pesait 22,3 grammes. 6,35 grammes supplémentaires ont été obtenus par évaporation de la liqueur mère, donnant ainsi un total de 28,65 grammes (96,0 %). |
| Marque | Ancobon (Valant). |
| Fonction thérapeutique | Antifongique |
| Activité anti-microbienne | Le spectre d'activité est limité à Candida spp., Cryptococcus spp. et certains champignons provoquant la chromoblastomycose. |
| Résistance acquise | Environ 2 à 3 Candida spp. les isolats (plus nombreux dans certains centres) sont résistants avant le début du traitement, et une résistance peut se développer pendant le traitement. La cause la plus fréquente de résistance semble être la perte de l’enzyme uridine monophosphate pyrophosphorylase. |
| Applications pharmaceutiques | Une pyrimidine fluorée synthétique disponible pour perfusion intraveineuse ou administration orale. |
| Actions Biochimie/Physiol | Analogue nucléosidique ayant des activités antifongiques. 5-FC est désaminé par la cytosine désaminase pour produire du 5-fluorouracile, ce qui entraîne un codage erroné de l'ARN. 5-La fluorocytosine inhibe la synthèse de l'ADN et de l'ARN et interfère avec la synthèse des protéines ribosomales. |
| Mécanisme d'action | La flucytosine (5-flucytosine, 5-FC ; Ancoban) est un analogue de pyrimidine fluorée de la cytosine qui a été initialement synthétisé pour une utilisation éventuelle comme agent antinéoplasique. Il est indiqué uniquement pour le traitement des infections systémiques graves causées par des souches sensibles de Candida et Cryptococcus spp. Le mécanisme d'action de la 5-fluorocytosine (5-FC) a été étudié en détail. Le médicament entre dans le cellule fongique par transport actif sur les ATPases qui transportent normalement les pyrimidines. Une fois à l'intérieur de la cellule, la 5-fluorocytosine est désaminé dans une réaction catalysée par la cytosine désaminase pour produire du 5-fluorouracile (5-FU). 5-Le fluorouracile est le métabolite actif du médicament.5-Le fluorouracile entre dans les voies de synthèse des ribonucléotides et des désoxyribonucléotides. Les fluororibonucléotidetriphosphates sont incorporés dans l'ARN, provoquant une synthèse défectueuse de l'ARN. Cette voie provoque la mort cellulaire. Dans la série des désoxyribonucléotides, le 5-fluorodésoxyuridinemonophosphate (F-dUMP) se lie à l'acide 5,10-méthylènetétrahydrofolique, interrompant le substrat du pool à un carbone qui alimente la synthèse du thymidylate. La synthèse de l’ADN est donc bloquée. |
| Pharmacologie | 5-FC est bien absorbé par voie orale, avec une biodisponibilité supérieure à 90 %. La demi-vie sérique est de 3 à 5 heures, avec des taux sériques culminant de 4 à 6 heures après une dose unique. Le médicament est largement distribué dans les fluides corporels, avec des taux de liquide céphalo-rachidien représentant 60 à 80 % des taux sériques. Le médicament pénètre également bien. dans l'urine, l'humeur aqueuse et les sécrétions bronchiques. La liaison minimale aux protéines sériques permet à plus de 90 % de chaque dose d'être excrétée dans l'urine ; des réductions significatives de la posologie sont nécessaires en présence d'insuffisance rénale. 5-FC peut être éliminé à la fois par hémodialyse et par dialyse péritonéale. La conversion des 5-FC en métabolites toxiques peut se produire dans une mesure limitée dans les cellules de mammifères, ce qui explique la toxicité des 5-FC. |
| Pharmacocinétique | Absorption orale : Complète Cmaximum25 mg/kg 6-heure par voie orale : 70 à 80 mg/L après 1 à 2 heures Demi-vie plasmatique : 3 à 6 heures Volume de distribution : 0,7–1 L/kg Liaison aux protéines plasmatiques c. 12% L'absorption est plus lente chez les personnes souffrant d'insuffisance rénale, mais les concentrations maximales sont plus élevées. Les niveaux dans le LCR représentent environ 75 % de la concentration sérique simultanée. Plus de 90 % d'une dose de flucytosine est excrétée dans l'urine sous forme inchangée. La demi-vie sérique est beaucoup plus longue en cas d'insuffisance rénale, ce qui nécessite une modification du schéma posologique : pour les patients ayant une clairance de la créatinine inférieure à 40 ml/min, l'intervalle posologique doit être doublé à 12 h ; En cas d'insuffisance rénale sévère, l'intervalle posologique doit être encore augmenté jusqu'à une fois par jour ou moins, sur la base de mesures fréquentes de la concentration sérique du médicament. |
| Utilisation clinique | La flucytosine a une activité antifongique significative contre C. albicans, d'autres espèces de Candida, C. neoformans et les organismes fongiques responsables de la chromomycose. Non considéré comme le médicament de choix pour ces infections fongiques, le 5-FC reste utile dans le cadre d'une thérapie combinée pour la candidose systémique et la méningite cryptococcique et comme médicament alternatif pour la chromomycose. Lorsqu’il est utilisé en monothérapie, les résistances et les échecs cliniques sont fréquents. Les mécanismes potentiels de résistance aux médicaments comprennent une diminution de la perméabilité de la membrane cellulaire fongique et une réduction des niveaux de cytosine désaminase fongique. La thérapie combinée avec l'amphotéricine B et la flucytosine dans le traitement de la méningite cryptococcique et des infections profondes à Candida, telles que l'arthrite septique et la méningite, permet de réduire le dosage de l'amphotéricine B et prévient l'émergence d'une résistance au 5-FC. Lorsque des doses plus élevées d'amphotéricine B sont utilisées, la thérapie combinée avec 5-FC ne confère aucun bénéfice clinique supplémentaire, sauf dans le traitement de l'endophtalmie à Candida, où la pénétration tissulaire reste problématique. |
| Utilisation clinique | Candidose (en association avec l'amphotéricine B ou le fluconazole) Cryptococcose (en association avec l'amphotéricine B ou le fluconazole) La surveillance des concentrations de flucytosine est souhaitable chez tous les patients et obligatoire chez ceux présentant une insuffisance rénale. |
| Effets secondaires | Les nausées, les vomissements, les douleurs abdominales et la diarrhée sont fréquents. Les effets secondaires graves comprennent la myélosuppression et la toxicité hépatique ; ils surviennent plus fréquemment lorsque les concentrations sériques dépassent 100 mg/L. Les effets néphrotoxiques de l'amphotéricine B peuvent entraîner des concentrations sanguines élevées de flucytosine, et les taux de ce dernier médicament doivent être surveillés lorsque ces composés sont administrés ensemble. Lorsque 5-FC est prescrit seul à des patients présentant une fonction rénale normale, une éruption cutanée, une détresse épigastrique, une diarrhée et une élévation des enzymes hépatiques peuvent survenir. |
| La synthèse | La flucytosine, 5-fluorocytosine (35.4.4), est synthétisée à partir du fluorouracile (30.1.3.3). Le fluorouracile réagit avec l'oxychlorure de phosphore dans la diméthylaniline pour former la 2,4-dichloro-5-fluoropyrimidine (35.4.2), qui réagit avec l'ammoniac pour former un produit substitué par du chlore en quatrième position du cycle pyrimidine. —4-amino- 2-chloro-5-fluoropyrimidine (35.4.3). L'hydrolyse du fragment chlorovinylique de ce composé dans une solution d'acide chlorhydrique donne la flucytosine recherchée.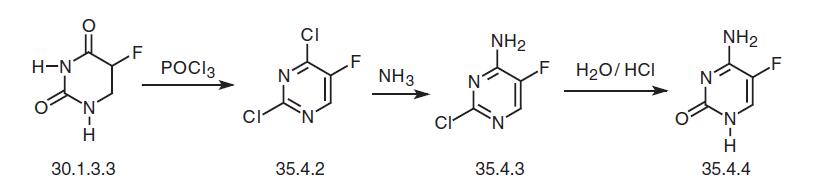 Une autre méthode de synthèse consiste à fabriquer de la flucytosine à partir d'un précurseur du fluorouracile — 5-fluoro-2-méthylthiouracile (30.1.3.2) en utilisant un schéma quelque peu analogue. Le traitement du 5-fluoro-2-méthylthiouracile (30.1.3.2) avec du pentachlorure de phosphore donne du 4-chloro-5-fluoro-2-méthylthiopyrimidine (35.4.5), qui, après réaction avec l'ammonium est transformé en 4-amino-5-fluoro-2-méthylthiopyrimidine (35.4.6). L'hydrolyse du fragment méthylthiovinyle à l'aide d'acide bromhydrique concentré donne la flucytosine souhaitée. 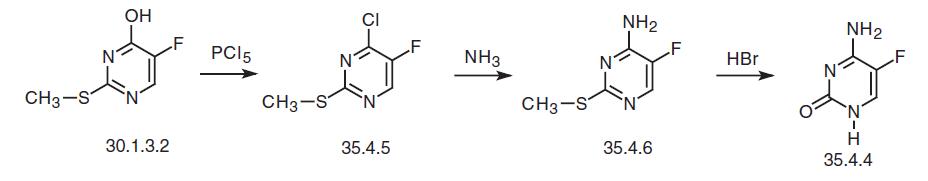 |
| Interactions médicamenteuses | Interactions potentiellement dangereuses avec d'autres médicaments Cytarabine : concentration de flucytosine éventuellement réduite. |
| Métabolisme | La flucytosine elle-même n'est pas cytotoxique mais est plutôt un promédicament qui est absorbé par les champignons et métabolisé en 5-fluorouracile (5-FU) par la cytidine désaminase fongique. Ensuite, le 5-FU est converti en 5-fluorodésoxyuridine, qui, en tant qu'inhibiteur de la thymidylate synthase, interfère avec la biosynthèse des protéines et de l'ARN. 5-Le fluorouracile est cytotoxique et est utilisé en chimiothérapie anticancéreuse. Les cellules humaines ne contiennent pas de cytosine désaminase et ne convertissent donc pas la flucytosine en 5-FU. Cependant, certaines flores intestinales convertissent le médicament en 5-FU, de sorte que la toxicité humaine résulte de ce métabolisme. |
| Produits de préparation de fluorocytosine et matières premières |
| Matières premières | Phosphorus oxychloride-->N-Methylaniline-->5-Fluorouracil-->4-Amino-2-chloro-5-fluoropyrimidine-->2,4-Dichloro-5-fluoropyrimidine-->5-FLUORO-4-HYDROXY-2-METHOXYPYRIMIDINE-->Oxychlorure de phosphore |
| Produits de préparation | 2',3'-Di-O-acétyl-5'-désoxy-5-fuluro-D-cytidine |
étiquette à chaud: fluorocytosine, fabricants, fournisseurs, usine de fluorocytosine en Chine
Vous pourriez aussi aimer
Envoyez demande







