
Présentation du produit
| Informations de base sur le fluorure de calcium |
| Propriétés chimiques Structure cristalline Utilisations Méthode de production |
| Nom du produit: | Fluorure de calcium |
| Synonymes: | Fluorure de calcium;Fluorure de calcium, 99,9 % à base de traces de métaux;Fluorure de calcium, 99,95 % à base de traces de métaux;Fluorure de calcium, anhydre, ampoule sous argon, 99,99 % à base de traces de métaux;Fluorure de calcium en Chine;Anticorps ANTI-CNOT8 (C-TERM) produit chez le lapin;Protéine de type CAF1-;CALIFp |
| CAS: | 7789-75-5 |
| FM: | CaF2 |
| MW: | 78.07 |
| Institut national de statistique de l'UNESCO: | 232-188-7 |
| Catégories de produits : | Inorganiques;halogénures métalliques |
| Fichier Mol: | 7789-75-5.mol |
 |
|
| Propriétés chimiques du fluorure de calcium |
| Point de fusion | 1402 degrés |
| Point d'ébullition | 2500 degrés (littéralement) |
| densité | 3,18 g/mL à 25 degrés (lit.) |
| indice de réfraction | 1.434 |
| Fp | 2500 degrés |
| température de stockage | -20 degré |
| solubilité | Légèrement soluble dans l'acide; insoluble dans l'acétone. |
| formulaire | tige |
| couleur | blanc |
| Densité spécifique | 3.18 |
| Solubilité dans l'eau | 0.015 g. pour 100 g d'eau à température ambiante.(INSOLUBLE) |
| Sensible | Hygroscopique |
| Merck | 14,1667 |
| Constante du produit de solubilité (Ksp) | pKsp: 8,28 |
| Limites d'exposition | ACGIH : TWA 2,5 mg/m3 NIOSH : IDLH 250 mg/m3 ; VME 2,5 mg/m3 |
| Constante diélectrique | 2.5 (ambiant) |
| Stabilité: | Stable. Le fluorure de calcium est inerte vis-à-vis des produits chimiques organiques et de nombreux acides, dont le HF. Il se dissout lentement dans l'acide nitrique. |
| Clé InChI | WUKWITHWXAAZEY-UHFFFAOYSA-L |
| Référence de la base de données CAS | 7789-75-5(Référence de la base de données CAS) |
| Référence en chimie du NIST | Fluorure de calcium (7789-75-5) |
| Système de registre des substances de l'EPA | Difluorure de calcium (7789-75-5) |
| Consignes de sécurité |
| Codes de danger | Xi, Xn |
| Déclarations de risque | 36/37/38 |
| Déclarations de sécurité | 26-37/39-36 |
| RIDADR | 3288 |
| WGK Allemagne | 1 |
| RTEC | EW1760000 |
| Avis de danger | Irritant |
| TSCA | Oui |
| Code SH | 28261900 |
| Données sur les substances dangereuses | 7789-75-5(Données sur les substances dangereuses) |
| Toxicité | DL50 ip chez la souris : 2638,27 mg/kg (Stratmann) |
| Informations sur la fiche signalétique |
| Fournisseur | Langue |
|---|---|
| Fluorure de calcium | Anglais |
| SigmaAldrich | Anglais |
| ACROS | Anglais |
| ALFA | Anglais |
| Utilisation et synthèse du fluorure de calcium |
| Propriétés chimiques | Le fluorure de calcium est le principal ingrédient du spath fluor ou de la fluorite, la formule chimique est CaF2, c'est un cristal cubique incolore ou une poudre blanche. La densité relative est de 3,18, le point de fusion est de 1423 degrés, le point d'ébullition est d'environ 250 degrés. La solubilité dans l'eau est minime, 100 g d'eau ne peuvent dissoudre que 0,0016 g à 18 degrés, il est insoluble dans l'acétone, mais soluble dans l'acide chlorhydrique, l'acide fluorhydrique, l'acide sulfurique, l'acide nitrique et une solution de sel d'ammonium, et il ne peut pas réagir avec l'acide dilué, mais peut réagir avec l'acide sulfurique concentré chaud et générer de l'acide fluorhydrique, il peut former un complexe lorsqu'il se dissout dans une solution de sels d'aluminium et de fer (Fe3 +). Le fluorure de calcium naturel est un minéral fluoré ou spath fluor, qui présente souvent des couleurs grises, jaunes, vertes, violettes et autres, parfois il est incolore, transparent, brillant, cassant et sa densité relative est de 3,01 à 3,25, il présente un phénomène de fluorescence important. Il peut être utilisé comme source de fluor et comme matériau pour fabriquer un système d'acide fluorhydrique, du fluorure ; et il peut également être utilisé dans la fabrication de verre, d'émail, de glaçure. La fluorite est principalement utilisée comme fondant dans la métallurgie, le spath fluor très pur peut être utilisé pour fabriquer des lentilles spéciales. L'eau contenant (1 à 1,5) × 10-6 de fluorure de calcium peut prévenir les problèmes dentaires. De plus, il peut être utilisé dans la fusion du fer et de l'acier, la fabrication de produits chimiques, de verre et de céramique. Le produit pur peut être utilisé comme catalyseur de déshydratation, de déshydrogénation. Par l'effet de sels de calcium solubles (carbonate de calcium ou hydroxyde de calcium) et de fluorure de sodium ou d'acide fluorhydrique, on peut obtenir du fluorure d'ammonium, du fluorure de calcium. |
| structure cristalline | Le fluorure de calcium est un cristal ionique dont les anions fluor sont disposés dans un réseau cubique simple et les cations calcium dans la moitié des sites cubiques de la structure. Les ions calcium peuvent également être considérés comme étant sur un réseau fcc « étendu » avec les ions fluor provoquant leur séparation de réseau à 0,39 nm. Cette représentation est illustrée dans le diagramme inférieur. La maille unitaire contient 4 Ca2+ions et 8 F1-ions.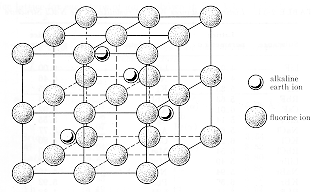 Le matériau est transparent dans la région spectrale visible et présente une adsorption optique électronique dans l'ultraviolet et une absorption optique en réseau dans l'infrarouge. |
| Utilisations |
Industrie
Application
Rôle/avantage
Fabrication de produits chimiques
Production d'acide fluorhydrique et de fluorure
Matière première/source de fluorure
Production de produits chimiques fins à base de fluor et de cryolite synthétique
Matière première/source de fluorure
Matériau architectural
Production de verre
Agent fondant/favorise la fusion des matières premières
Production de ciment
Agent de minéralisation
Production de glaçure céramique
Flux et colorants
Métallurgie
Fusion de fer et d'acier, production de ferroalliages, etc.
Agent fondant/réduit le point de fusion des substances réfractaires
Médecine
Traitement, contrôle, prévention et amélioration des réactions allergiques
Favoriser la formation de nouveaux os
Systèmes d'imagerie thermique, spectroscopie, télescopes et lasers excimères
Fabrication de composants optiques, tels que fenêtres et lentilles
Matière première / large gamme de fréquences de transmission de la lumière ; faible indice de réfraction ; stabilité thermique élevée
Autres
Production d'agents de soudage
Composants importants dans les revêtements des baguettes de soudage et des poudres de soudage
Réaction de déshydratation et de déshydrogénation
Catalyseur/accélère le processus de réaction
Fabrication de garnitures de frein
Additif/aide à réduire l'abrasion causée par la chaleur élevée et la friction
|
| Méthode de production | Les gisements de fluorite découverts en Chine sont principalement exploités par des mines souterraines, ou par des mines à ciel ouvert peu profondes, et par des mines souterraines profondes, pour lesquelles la plupart des veines du corps minéralisé sont inclinées, et dont l'extension est également importante. La méthode d'extraction est basée sur la méthode de retrait par trou peu profond. Le processus d'extraction est basé sur la « roche phosphatée ». Les méthodes de valorisation sont généralement de deux types, la première consiste à transformer le minerai brut en concentré de minerai qualifié par sélection de traitement, la seconde consiste à sélectionner manuellement le minerai maigre et les résidus. |
| Description | Le fluorure de calcium est une substance cristalline incolore ou blanche, sous forme de poudre. Poids moléculaire : 8 ; densité (H2O : 1) : 4 ; 18 à 20 degrés ; point d'ébullition : 7 degrés ; point de congélation/fusion : 8 degrés. Identification des dangers (basée sur le système de notation NFPA : M) : santé : 2, inflammabilité : 0, réactivité : 0. Pratiquement insoluble dans l'eau. |
| Propriétés chimiques | Le fluorure de calcium, CaF2, également connu sous le nom de fluorite et de feldspath, est un solide incolore composé de cristaux cubiques. Il a une faible solubilité dans l'eau, mais est facilement soluble dans les solutions de sel d'ammonium. Le fluorure de calcium est utilisé dans la synthèse de l'acide fluorhydrique et dans la gravure du verre. Le fluorure de calcium n'est pas hygroscopique et est relativement inerte. Il présente une résistance suffisamment élevée aux chocs thermiques et mécaniques et peut être facilement transformé en une variété de géométries de détecteurs. Le fluorure de calcium a une pression de vapeur très faible, ce qui lui permet d'être utilisé dans une grande variété d'applications sous vide. Il est insoluble dans l'eau et la plupart des solvants organiques, ce qui permet de mettre en contact direct des échantillons radioactifs en solution avec le cristal. Le fluorure de calcium est un matériau transparent utilisé pour détecter les rayons α jusqu'à plusieurs centaines de keV et pour détecter les particules chargées. En raison de son faible numéro atomique, la photofraction du matériau est relativement faible, ce qui limite son utilisation en spectrométrie à rayons α à des énergies plus élevées. Cependant, le faible numéro atomique fait du fluorure de calcium un matériau idéal pour la détection des particules α en raison de la faible quantité de rétrodiffusion. |
| Propriétés physiques | Cristal ou poudre cubique blanc ; indice de réfraction 1,434 ; densité 3,18 g/cm3 ; dureté 4 Mohs ; fond à 1 418 degrés ; se vaporise à 2 533 degrés ; insoluble dans l'eau (16 mg/L à 20 degrés) ; Ksp 3,9x10-11 ; légèrement soluble dans l'acide minéral dilué ; soluble dans les acides concentrés (avec réaction). |
| Utilisations | Le CaF2 naturel est la principale source de fluorure d'hydrogène, un produit chimique de base utilisé pour produire une large gamme de matériaux. Le fluor est libéré du minéral par l'action de l'acide sulfurique concentré : CaF2 (solide)+H2SO4 (liq)→CaSO4 (solide)+2HF (gaz) Le CaF2 est utilisé comme composant optique en raison de sa stabilité chimique dans des conditions défavorables. Le fluorure de calcium est couramment utilisé comme matériau de fenêtre pour les longueurs d'onde infrarouges et ultraviolettes, car il est transparent dans ces régions (environ 0.15 à 9 mm) et présente un indice de réfraction extrêmement faible. Le fluorure de calcium est une source de calcium insoluble dans l'eau destinée à être utilisée dans des applications sensibles à l'oxygène, telles que la production de métaux. À des concentrations extrêmement faibles (ppm), les composés fluorés sont utilisés dans des applications de santé. Les composés fluorés ont également des utilisations importantes en chimie organique synthétique. Ils sont également couramment utilisés pour l'alliage des métaux et pour le dépôt optique. Il est également utilisé comme fondant pour la fusion et le traitement liquide du fer, de l'acier et de leurs composés. Son action repose sur son point de fusion similaire à celui du fer, sur sa capacité à dissoudre les oxydes et sur sa capacité à mouiller les oxydes et les métaux. |
| Utilisations | Le spath fluor est la principale source primaire de fluor et de ses composés. Dans la métallurgie ferreuse, il est utilisé comme fondant pour augmenter la fluidité des scories. L'industrie sidérurgique en est le plus grand consommateur, l'industrie chimique, le deuxième, et l'industrie du verre et de la céramique, le troisième. Le spath fluor synthétique est utilisé dans l'industrie optique (transmet les rayons UV) et le fluorure de calcium pur est utilisé comme catalyseur dans la déshydratation et la déshydrogénation. Il est utilisé pour fluorer l'eau potable. |
| Utilisations | Le fluorure de calcium est une source commerciale importante de composés fluorés ainsi que de fluorure d'hydrogène. Il est transparent de l'ultraviolet à l'infrarouge. Il est utilisé en spectroscopie, dans les systèmes d'imagerie thermique et dans les lasers à excimères. Il est également utilisé dans la fabrication de composants optiques, notamment les fenêtres, les prismes et les lentilles. En outre, il est également utilisé dans la métallurgie de l'aluminium, dans les industries de fabrication de garnitures de freins et dans l'émail des dents. |
| Définition | Une forme pure et naturelle de fluorure de calcium. |
| Méthodes de production | Le produit commercial est obtenu à partir de fluorite minérale naturelle, purifiée et réduite en poudre. Il peut également être précipité en mélangeant une solution de fluorure de sodium avec un sel de calcium soluble : Ca(NO3)2+ 2NaF → CaF2+ NaNO3 Alternativement, il peut être obtenu en traitant le carbonate de calcium avec de l'acide fluorhydrique : CaCO3+ 2HF → CaF2+ CO2 + H2O. |
| Définition | Une forme minérale de fluorure de calcium (CaF2), utilisé dans la fabrication de certains ciments et types de verre. |
| Description générale | Poudre ou granulés gris inodores. Pénètre dans l'eau. |
| Profil de réactivité | Le fluorure de calcium a un faible pouvoir oxydant ou réducteur. Des réactions d'oxydoréduction peuvent néanmoins se produire. La majorité des composés de cette classe sont légèrement solubles ou insolubles dans l'eau. Si elles sont solubles dans l'eau, les solutions ne sont généralement ni fortement acides ni fortement basiques. Ces composés ne réagissent pas avec l'eau. |
| Danger | Un irritant. |
| Danger pour la santé | Peu de toxicité aiguë |
| Inflammabilité et explosibilité | Non inflammable |
| Utilisations industrielles | Également appelé fluorite, le spath fluor est un minéral cristallin ou granulaire massif de composition CaF2, utilisé comme fondant dans la fabrication de l'acier, pour la fabrication de l'acide fluorhydrique, dans le verre opalescent, dans les émaux céramiques, pour le lissage de la cryolite artificielle, comme liant pour les meules abrasives vitreuses et dans la production de ciment blanc. C'est un meilleur fondant pour l'acier que le calcaire, car il permet de produire un laitier fluide et de libérer le fer du soufre et du phosphore. Le spath acide est une qualité utilisée dans la fabrication de l'acide fluorhydrique. Il est également utilisé pour la fabrication de réfrigérants, de plastiques et de produits chimiques, ainsi que pour la réduction de l'aluminium. Le spath fluor optique est la qualité la plus élevée, mais il n'est pas courant. Les cristaux de fluorure pour lentilles optiques sont cultivés artificiellement à partir de spath fluor de qualité acide. Fluorure de calcium pur, Ca2F6, est une poudre cristalline incolore utilisée pour graver le verre, dans les émaux et pour réduire la friction dans les roulements des machines. Il est également utilisé pour les pièces en céramique résistantes à l'acide fluorhydrique et à la plupart des autres acides. La fluorite de calcium contient du silicium dans la molécule et est une poudre cristalline utilisée pour les émaux. Les cristaux de fluorure rhombiques clairs utilisés pour transformer l'énergie électrique en lumière sont le fluorure de plomb, PbF2. |
| Profil de sécurité | Modérément toxique par voie intrapéritonéale. Légèrement toxique par ingestion. Tératogène expérimental. Autres effets expérimentaux sur la reproduction. Données de mutation signalées. Voir également FLUORURES et COMPOSÉS DU CALCIUM. Lorsqu'il est chauffé jusqu'à décomposition, il émet des fumées toxiques de F-. |
| Exposition potentielle | Le fluorure de calcium est utilisé pour la production d'acide fluorhydrique, comme fondant dans la fabrication de l'acier, dans la fusion, dans le soudage à l'arc électrique, dans la fabrication du verre et de la céramique, et pour fluorer l'eau potable. |
| PREMIERS SECOURS | Si ce produit chimique entre en contact avec les yeux, retirez immédiatement toutes les lentilles de contact et irriguez immédiatement pendant au moins 15 minutes, en soulevant de temps en temps les paupières supérieures et inférieures. Consultez immédiatement un médecin. Si ce produit chimique entre en contact avec la peau, retirez les vêtements contaminés et lavez-vous immédiatement avec de l'eau et du savon. Consultez immédiatement un médecin. Si ce produit chimique a été inhalé, éloignez-le de l'exposition, commencez la respiration artificielle (en utilisant les précautions universelles, y compris le masque de réanimation) si la respiration s'est arrêtée et la réanimation cardiopulmonaire si le rythme cardiaque s'est arrêté. Transférez rapidement vers un établissement médical. Si ce produit chimique a été avalé, consultez un médecin. Un médecin ou un ambulancier autorisé peut envisager d'administrer du gel d'hydroxyde d'aluminium, si la personne est consciente. |
| stockage | Code couleur vert : un stockage général peut être utilisé. Conserver dans des récipients hermétiquement fermés dans un endroit frais et bien ventilé, à l'écart des acides et des métaux chimiquement actifs (tels que le potassium, le sodium, le magnésium et le zinc), car du fluorure d'hydrogène corrosif sera produit. |
| Expédition | Le fluorure de calcium n’est pas spécifiquement couvert par le DOT dans ses normes d’emballage axées sur les performances. |
| Incompatibilités | La poussière peut former un mélange explosif avec l'air. Réagit avec l'eau, l'air humide et la vapeur, libérant de l'hydrogène gazeux inflammable ; et peut s'auto-enflammer dans l'air. Agent réducteur puissant ; incompatible avec les oxydants (chlorates, nitrates, peroxydes, permanganates, perchlorates, chlore, brome, fluor, etc.) ; le contact peut provoquer des incendies ou des explosions. Tenir à l'écart des matières alcalines, des bases fortes, des acides forts, des oxoacides, des époxydes. Incompatible avec les halogénates métalliques, le fluorure d'argent et le tétrahydrofurane |
| Produits de préparation et matières premières à base de fluorure de calcium |
| Matières premières | Hydrogen fluoride-->Calcium hydroxide-->CARBON MONOXIDE-->Quartz-->Calcium acetate-->phosphate de calcium et de magnésium (CMP) |
| Préparation des produits | Hydrogen fluoride-->Boron trifluoride diethyl etherate-->Potassium Phosphate Monobasic-->Hexafluorosilicic acid-->Calcium cyanamide-->Sodium fluoride-->Trisodium hexafluoroaluminate-->Aluminum fluoride-->bastnasite-->Carbon tetrafluoride-->cryolite-->ZINC SILICOFLUORIDE-->HEXAFLUOROACÉTYLACÉTONATE DE MAGNÉSIUM DIHYDRATÉ |
étiquette à chaud: fluorure de zinc, fabricants et fournisseurs de fluorure de zinc en Chine, usine
Une paire de: Fluorure de zirconium
Un article: Fluorure de calcium
Vous pourriez aussi aimer
Envoyez demande


