| Description |
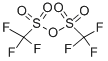
L'anhydride trifluorométhanesulfonique, également connu sous le nom d'anhydride triflique, s'est révélé être un réactif extraordinaire pour un large éventail de transformations. En tant que réactif disponible dans le commerce et facilement disponible, il a été largement utilisé en chimie de synthèse en raison de sa forte électrophilie. Compte tenu de sa forte affinité pour les O-nucléophiles, la réaction avec les alcools, les carbonyles, les oxydes de soufre, de phosphore et d'iode vers la formation des triflates correspondants est fortement favorisée. En tant que l'un des principaux groupes partants en chimie organique, les triflates générés ouvrent ensuite la porte à diverses transformations en aval, y compris (mais sans s'y limiter) des réactions de substitution, des processus de couplage croisé, des réactions redox et des réarrangements[1-2] . |
| Propriétés chimiques |
liquide clair, incolore à brun clair |
| Les usages |
L'anhydride trifluorométhanesulfonique est un électrophile puissant utilisé en synthèse chimique pour introduire le groupe triflyle. |
| Les usages |
L'anhydride trifluorométhanesulfonique est utilisé pour convertir les phénols et l'imine en ester triflique et en groupe NTf. C'est un électrophile puissant utilisé pour l'introduction du groupe triflyle en synthèse chimique. Il sert de réactif dans la préparation de triflates d'alkyle et de vinyle et pour la synthèse stéréosélective de donneurs de mannosazide méthyl uronate. Il agit comme un catalyseur de glycosylation avec des sucres hydroxyles anomériques pour préparer des polysaccharides. |
| Définition |
ChEBI : L'anhydride triflic est un anhydride organosulfonique. Il est fonctionnellement lié à un acide triflique. |
| Profil de réactivité |
L'activation électrophile d'amides tertiaires et secondaires avec l'anhydride triflique (Tf2O ; anhydride rifluorométhanesulfonique) dans des conditions douces donne naissance respectivement à des triflates d'iminium et d'imino, qui pourraient être utilisés comme réactifs polyvalents pour réagir avec divers C-, N-, O- et S. -des nucléophiles pour la transformation d'une fonction amide en différents produits. D'autres nucléophiles contenant de l'oxygène, tels que les sulfoxydes et les oxydes de phosphore, pourraient également subir une attaque nucléophile avec Tf2O pour générer du triflate de thionium, des espèces P électrophiles et du triflate de phosphonium. Ces espèces transitoires très actives pourraient facilement subir des réactions de substitution nucléophile pour d’autres transformations diverses. De plus, en raison de sa forte propriété électrophile, Tf2O a tendance à réagir avec des nucléophiles relativement faibles tels que les groupes nitrile ou certains composés hétérocycliques contenant de l'azote. De plus, Tf2O a également été utilisé comme réactif efficace de trifluorométhylation radicalaire et de trifluorométhylthiolation grâce à la libération de SO2 ou à un processus de désoxygénation pour la synthèse de composés trifluorométhylés et trifluorométhylthiolés[2]. |
| Danger |
Peut être corrosif pour les métaux. Nocif en cas d'ingestion. Provoque de graves brûlures de la peau et des lésions oculaires. |
| Inflammabilité et explosibilité |
Non classés |
| La synthèse |
La synthèse de l'anhydride trifluorométhanesulfonique est la suivante :
Un ballon sec de {{0}} ml. à fond rond est chargé de 36,3 g. (0,242 mole) d'acide trifluorométhanesulfonique (Note 1) et 27,3 g. (0,192 mole) de pentoxyde de phosphore (Note 2). Le flacon est bouché et laissé au repos à température ambiante pendant au moins 3 heures. Pendant cette période, le mélange réactionnel passe d’une bouillie à une masse solide. Le ballon est équipé d'une tête de distillation à court trajet et chauffé d'abord avec un flux d'air chaud provenant d'un pistolet thermique, puis avec la flamme d'un petit brûleur.Le ballon est chauffé jusqu'à ce qu'il n'y ait plus d'anhydride trifluorométhanesulfonique distillé, point d'ébullition 82-115 degrés, ce qui donne 28,4-31,2 g. (83 à 91 %) de l'anhydride, un liquide incolore. Bien que ce produit soit suffisamment pur pour être utilisé dans l'étape suivante, l'acide restant peut être éliminé de l'anhydride par la procédure suivante. Une bouillie de 3,2 g. de pentoxyde de phosphore dans 31,2 g. de l'anhydride brut est agité à température ambiante dans un ballon bouché pendant 18 heures. Une fois que le ballon de réaction a été équipé d'une tête de distillation à court trajet, il est chauffé avec un bain d'huile, ce qui donne 0,7 g. du premier coup, pb 74–81 degrés, suivi de 27,9 g. de l'anhydride d'acide trifluorométhanesulfonique pur, point d'ébullition 81–84 degrés.

|
| stockage |
Conserver dans un endroit frais, sec et bien ventilé. Sensible à l'humidité. |
| Méthodes de purification |
Il peut être fraîchement préparé à partir de l'acide anhydre (11,5 g) et du P2O5 (11,5 g, soit la moitié de ce poids) en le laissant reposer 1 heure à température ambiante, en distillant les produits volatils puis en le distillant sur une courte colonne Vigreux. Il est facilement hydrolysé par H2O et se décompose sensiblement au bout de quelques jours pour libérer du SO2 et produire un liquide visqueux. Conservez-le au sec à basse température. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Les références |
[1] Haoqi Zhang. « Anhydride trifluorométhanesulfonique dans l'activation d'amide : un outil puissant pour forger des noyaux hétérocycliques. » TCIMAIL (2021).
[2] Dr Qixue Qin, Professeur Dr Ning Jiao, Zengrui Cheng. "Applications récentes de l'anhydride trifluorométhanesulfonique en synthèse organique." Angewandte Chemie 135 10 (2022). |